人类走过近 40 年的抗艾历程,迎来第 34 个艾滋病日。“终结不平等,终结艾滋病” 是 2021 年世界艾滋病日主题。
在联合国艾滋病规划署发布的《直面不平等 — 2021 艾滋病防治全球进展报告》中,2020 年约有 150 万新发艾滋病感染者,有 68 万死于艾滋病相关疾病。在 3770 万 HIV 感染者中,仍有 1020 万人无法获得有效的治疗。
目前公认疗效最佳的是抗逆转录病毒治疗,通过三种或三种以上的药物联合使用治疗艾滋病,该疗法能够减少单一用药产生的耐药性,最大限度抑制病毒的复制,也被称为鸡尾酒疗法。
国际上抗逆转录病毒药物共有 6 大类 30 多种药物(包括复方制剂),分别是核苷类逆转录酶抑制剂、非核苷类逆转录酶抑制剂、蛋白酶抑制剂、整合酶抑制剂、 融合抑制剂及 CCR5 抑制剂。
表 | 6 类抗逆转录病毒药物的作用机理(生辉根据公开资料整理)
根据 UNAIDS 统计,截止 2020 年末,全球范围内约 73% 的 HIV 病毒携带者及艾滋病患者接受了抗逆转录病毒治疗,与联合国制定的全球 90% 的艾滋病患者接受规范的抗逆转录病毒治疗的目标仍存在一定差距。
表 | 2015-2020 年全球接受抗逆转录病毒治疗人数(来源:UNAIDS)
随着鸡尾酒疗法的应用及普及,艾滋病逐渐由致死性疾病转变为慢性疾病。在早期发现、及时治疗且坚持服药的情况下,艾滋病感染者能够获得有尊严、有质量的生活,生存时间也大大延长,但该疗法也存在一定局限性,如药物带来的副作用。目前,全球各大药企也在积极的开发新药解决耐药及服药依从性差等问题。
表 | 抗 HIV 病毒药物在研管线(不含复方制剂)(生辉根据公开资料整理)
功能性治愈 HIV 或成短期目标
获得性免疫缺陷综合症(AIDS)也就是艾滋病, 是人类免疫缺陷病毒(HIV)引起的高病死率恶性传染病。HIV 是一种能够攻击人体免疫系统的病毒,主要攻击人体免疫系统中最重要的 CD4+T 淋巴细胞,最终导致人体细胞免疫功能丧失,引起各种机会性感染和肿瘤的发生。
HIV 感染人体后,会整合到免疫细胞的基因组中,成为 “前病毒”, 后利用细胞的机制进行自我复制。而部分被感染的免疫细胞会进入休眠状态,不产生新的 HIV 病毒,而是为病毒提供潜伏的场所,建立病毒储存库。
目前, 抗逆转录病毒治疗能够很好控制艾滋病,但并不能治愈艾滋病。因为药物治疗只能抑制病毒的复制,并不能清除病毒储存库,一旦停药,潜伏的病毒会重新激活并复制,因此患者需要终生服药。
HIV 储存库的存在,难以将 HIV 病毒彻底从人体体内清除达到治愈,功能性治愈成为退而求其次的目标,即在停止抗病毒治疗后,尽管病毒未能从体内被完全清除,但机体免疫能控制病毒而不出现临床相关症状和病情进展。
目前,全球研究者在功能性治愈艾滋病领域已进行了多种尝试,其中包括储存库 “激活与杀死” 与 “阻断并锁定”、基因编辑、广谱中和抗体、CAR-T 免疫细胞治疗等。
激活或抑制 HIV 病毒储存库
HIV 病毒储存库是治愈艾滋病主要的障碍,目前主要有两种功能性清除病毒储存库的策略治愈艾滋病,分别为 shock and kill 以及 block and lock。
图 | shock and kill 策略(来源:MDPI)
目前,已有 5 大类 300 多种化合物在体外试验中被发现可激活处于潜伏状态的病毒储存库,但清除效果却不理想。研究人员正探索使用多种潜伏期逆转剂协同作用(如组合使用 PCK 抑制剂与 BDR4 抑制剂),以提高清除率,同时降低对免疫细胞的毒性。
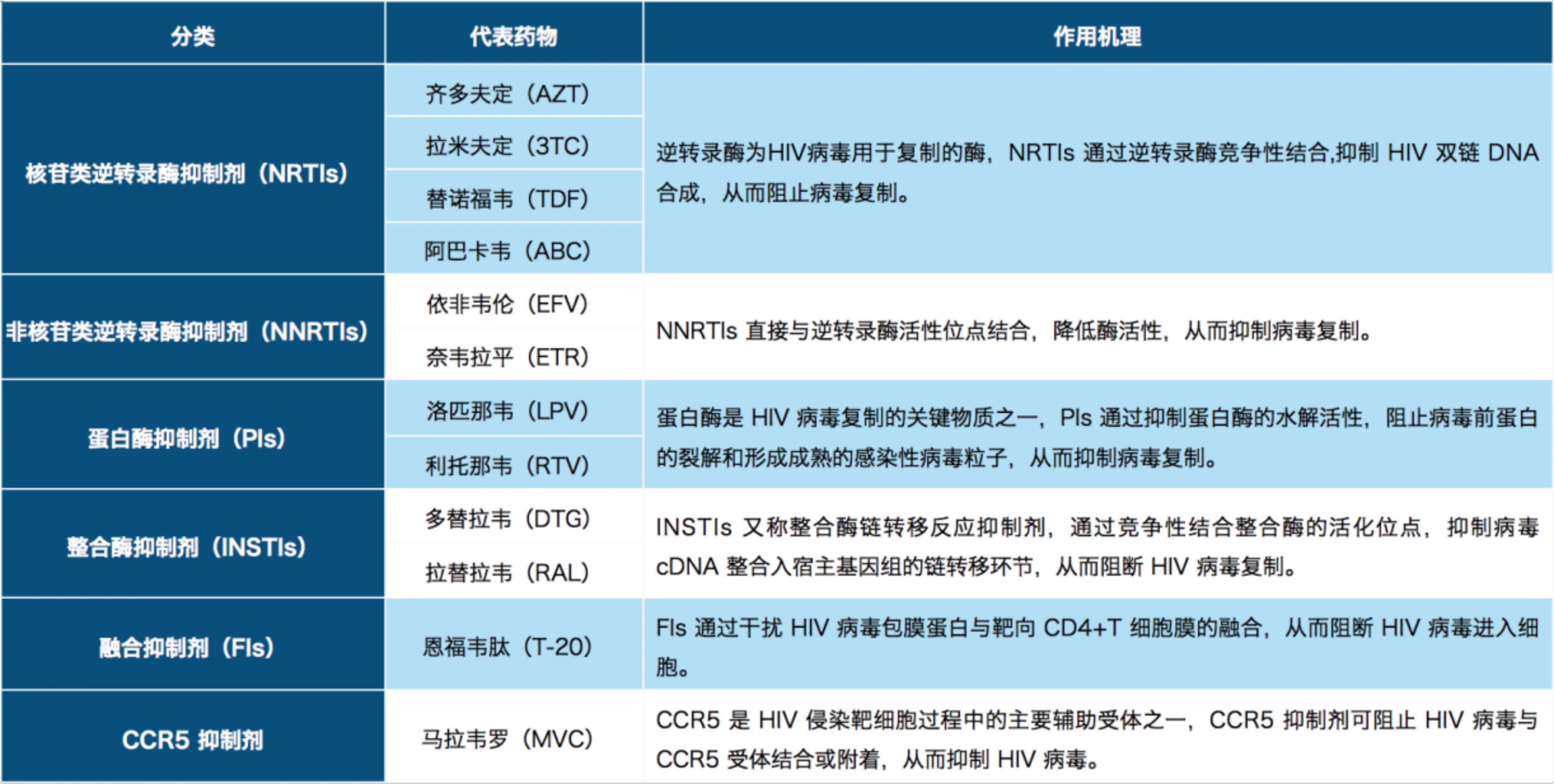
表 | 潜伏期激活剂分类(来源:European Journal of Medicinal Chemistry)
感染 HIV 患者中存在一小群 “精英控制者”,这部分人群能在不用服药的情况下,也能保持体内病毒复制长期处于抑制状态。block and lock 策略正是受其启发,利用潜伏促进药物(Latency Promoting Agents, LPAs),诱导病毒储存库处于深度潜伏状态,实现功能性治愈。
图 | block and lock 策略(来源:MDPI)
研究表明 Tat 蛋白可有效激活 HIV 基因的表达,因此被认为是促进药物开发的理想靶点。目前已发现一种天然化合物 didehydro-Cortistatin A (dCA)可作为 Tat 蛋白抑制剂,可使潜伏期的 HIV 继续潜伏,已在动物试验中取得成功。
基因编辑
HIV 病毒入侵免疫细胞的受体有两个,CD4 分子是第一受体,CCR5/CXCR4 是第二个受体(即辅助受体)。人类中有一少部分人因为 CCR5 受体基因与常人存在差异,丢失了其中的 32 个碱基对。HIV 病毒进攻人体后,因缺少进入人体细胞的辅助受体,无法进入人体细胞,直接被扼杀在摇篮。
“柏林病人” 与 “伦敦病人” 正是通过移植 CCR5 受体突变的供体骨髓,治愈了艾滋病。因只有少部分人存在 CCR5 受体基因突变,且骨髓移植是风险极大且昂贵的治疗手段,这两例成功治愈艾滋病患者的治疗方案并不具备普适性。
但这也启发了科学家开发基因疗法,包括不限于编辑 CCR5 受体基因使机体的 CD4+T 细胞缺失 HIV 病毒侵入的入口,或通过 CRISPR/Cas9 切割受感染细胞中的病毒基因,达到功能性治愈的目的。
在产业端,已有多家采用该路径的公司,就 HIV 的研究进入临床阶段。
2020 年 8 月,American Gene Technologies (AGT) 公司获得美国 FDA 的批准,开始一项名为 AGT103-T 细胞产品的 I 期临床试验,目的是通过基因疗法来消除艾滋病感染者体内的 HIV 病毒。AGT103-T 就是通过除掉 CD4 细胞上的 CCR5 受体治愈艾滋病,从而阻止 HIV 病毒进入 CD4 细胞。
2021 年 5 月,AGT103-T 完成了首次人体注射;2021 年 8 月,AGT 宣称 AGT103-T I 期试验安全无不良反应,将继续招募更多参与者。
Excision BioTherapeutics 是另外一家获得 FDA 批准启动 I/II 期临床试验的公司。EBT-101 是一款基于 CRISPR 技术的候选疗法,目的是功能性治愈 HIV-1 感染。
图 | EBT-101 基因疗法(来源:Excision BioTherapeutics)
广谱中和抗体
在人类与艾滋病病毒博弈的过程中,产生了一种特效抗击 HIV-1 病毒的成分 — 广谱中和抗体,其不仅可以通过直接中和病毒株,而且还能通过激发体内其它的免疫组分共同杀伤病毒,达到提升免疫力和杀伤病毒的目的。然而这类杀伤 HIV-1 病毒的利器在自然感染人体内产生非常困难,仅有少部分人有广谱中和抗体。随着越来越多的广谱中和抗体分离成功,研究者们开始探索将这些抗体应用于 HIV 的临床治疗中。
图 | 艾可宁 + 3BNC117 联合疗法(来源:前沿生物招股书)
采用抗体与长效治疗药物联用的方法,可以更大程度减少耐药和抗体逃逸株的产生,使得艾滋病病毒感染者无需每天服药,只需要数月或者半年注射一针就有可能实现较长时间的病毒抑制,这将极大提高病人用药依从性。
目前,前沿生物的艾可宁是中国唯一获批上市的抗 HIV 病毒长效注射药。艾可宁与广谱中和抗体 3BNC117 联合疗法正在美国开展 II 期临床试验。

CAR-T 细胞治疗
近年来,CAR-T 免疫细胞疗法在治疗血液瘤疾病中取得良好效果,在原理上也适用于艾滋病的治疗,因为 HIV 感染细胞也具有独特的表面特征。目前科学家已开始探索 CAR-T 细胞疗法治愈艾滋病的可能性。
图 | 张辉团队 CAR-T 疗法临床试验示意图(来源:JCI)
日前,中山大学张辉团队与和广州医科大学附属市八医院感染病中心合作,成功构建了对 HIV-1 感染的细胞具有特异性杀伤作用的 CAR-T 细胞,证实其可以特异性杀伤被 HIV-1 感染的细胞。在这个基础上,又合作开展了 CAR-T 细胞疗法清除 HIV-1 病毒储存库的 I 期临床研究,已经开展了接近 50 人次的回输试验。
安全性方面,受试者均能良好地耐受 CAR-T 细胞疗法,未发现明显不良反应;治疗效果方面,CAR-T 细胞疗法对血浆 HIV 病毒有一定抑制作用以及对 HIV 病毒储存库具有良好的清除作用。虽然病人停用抗病毒治疗后,还是出现了病毒反弹,但与历史对照相比,比不用 CAR-T 细胞疗法停药后反弹时间延长,且回输后 8 个月的 HIV 病毒储存库都较回输前减少。因 HIV 对 T 细胞的毒性及 HIV 受体多样性,下一步的研究不仅需要延长 CAR-T 细胞在体内存活的时间,同时需对 CAR 进行改装,使其善于发现 HIV 病毒的伪装并强化杀伤能力,以达到功能性治愈的目的。



