[摘要]一则“艾滋病病毒毒性减弱“的科研报告近几日在学术界引发轩然大波,在部分研究人员对此欢欣鼓舞之时,该项研究成果的可信度也引发了业界的争议。
一则“艾滋病病毒毒性减弱“的科研报告近几日在学术界引发轩然大波,在部分研究人员对此欢欣鼓舞之时,该项研究成果的可信度也引发了业界的争议。
今年“密西西比女孩”艾滋病病毒复发的事件给人们带来不小的打击,在抗击艾滋病的征途之上,任何科研、临床上的变化都能揪住人们的神经。而来自美国消息称:基因组剪辑技术已进入生物实验阶段这一科研进展或将扫去一些阴云。
12月,《美国国家科学院院刊》刊登了一份牛津大学研究团队的报告,报告声称,科研人员最新观测到,艾滋病病毒在与人体免疫系统对抗过程中发生演化,病毒正在逐渐适应人体的免疫能力,致病性和传染性均有所减弱,变得更加“温和”。
这一重大消息立刻引起人们关注。牛津大学该研究团队的Philip Goulder教授在接受BBC采访时解释说,病毒有时会攻入免疫系统健全的人的体内,那时候,病毒可能会被免疫系统消灭,而病毒如果要存活下去的话,就必须改变。这改变就是病毒的复制能力减弱艾滋病毒,使得病毒的传播能力也减少,引发艾滋病发病所需的时间也延长。
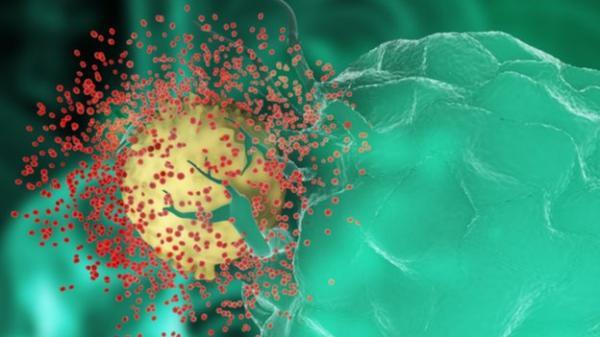
艾滋病病毒入侵模拟图,红色的艾滋病病毒正在入侵人体免疫细胞(黄色)
牛津大学的这一研究团队是在研究非洲国家博茨瓦纳和南非艾滋病发展历史时得出这一结论的。艾滋病病毒传入博茨瓦纳的时间要比传入南非早10年。研究人员在这两个国家选择超过2000名感染艾滋病病毒的女性艾滋病毒,观察和对比她们体内艾滋病病毒的变化。研究人员发现,在较早发现病毒的博茨瓦纳,病毒的复制能力比10年后发现病毒的南非减少了10%。
Philip Goulder教授在接受BBC采访时说:“这一发现太令人激动了。你可以观察到病毒的进化越来越缓慢,艾滋病病毒也许将被消除”。
Philip Goulder教授所在的研究团队还将这一结论刊登在《美国国家科学院院刊》上,报告还指出,目前对艾滋病病毒感染者进行的抗逆转录病毒治疗,也在促使艾滋病病毒的杀伤性减小。
这是因为用于抗逆转录病毒治疗(俗称“鸡尾酒疗法”)的药物,能够率先抑制艾滋病毒中较“难对付”的类型,使较温和的类型逐渐占据多数。研究人员通过数学模型推演得出结论:对免疫系统遭到破坏的艾滋病病毒感染者进行这种“选择性治疗”,能够使复制能力较低的艾滋病病毒加速发展,从而延缓发病。
牛津大学这一研究团队发现,20年前,艾滋病病毒感染者从感染到发病大约需要经过10年;而过去10年间,博茨瓦纳的艾滋病病毒感染者的发病时间,被推迟了大约2.5年。也就是说患者感染艾滋病病毒的潜伏期变成了12.5年。“这个增量的变化让我们开始期望,也许在未来,艾滋病感染者可能在十几年内都不会发病,呈现无病状的状态”,Philip Goulder教授说。
牛津大学的这一研究成果迅速在业界引发争议。不少一线抗击艾滋病的学者对此表示了怀疑。美国国立卫生研究院艾滋病中心主任Carl W.Dieffenbach教授12月4日在一场艾滋病研讨会时说:“这两天我已经接受了很多关于这个科研成果的咨询,但是从科研角度来看,我目前对此持谨慎态度,还没有大量数据支持,现在就判断艾滋病病毒毒性减弱显然太早了”。
复旦大学公共卫生学院一位教授告诉澎湃新闻(),目前医学上对艾滋病病毒采取的是如抗逆转录病毒治疗等一些治疗方式,对艾滋病病毒的致病性及病毒复制率都有所抑制,病毒是否进化得更加“温和”、以及与医疗干预之间的关系需要进一步验证和研究,而从理论证实到临床治疗更是有很长一段时间的距离。
上海市疾病预防控制中心终身教授康来仪也表示,结论不是艾滋病病毒毒性变温和这么简单,而且,还不清楚这项研究成果是针对艾滋病病毒1型还是2型。
当然,支持牛津大学这项研究的学者也不在少数,诺丁汉大学病毒学家Jonathan Ball教授就表示认同,“从理论上说,如果让艾滋病病毒自生自灭下去,经过漫长时间的跨度,病毒将对人无害。如果按照这种趋势发展下去,我们可以看到艾滋病病毒在全球范围内的传染力度慢慢下降。此外,人们采取的抗逆转录病毒疗法也会发挥类似的作用,最终我们将掌握抗击艾滋病病毒的主动权。”
虽然Philip Goulder教授所在团队认为艾滋病病毒毒性在减弱,但他也警告说:“虽然艾滋病病毒的复制能力在减低,但它不代表它没有杀伤力了。”
在抗击艾滋病的征途之上,任何科研、临床上的变化都能揪住人们的神经。今年“密西西比女孩”体内重新检测出艾滋病病毒的消息,又一次给了医学界沉重打击。这名未公布姓名的孩子被媒体称为“密西西比女孩”,2010年出生,因母婴传播,出生时即被诊断为感染有艾滋病病毒,在接受紧急治疗后,密西西比女孩体内的艾滋病病病毒降到常规检测无法发现的程度。科研人员认为这一结果有力地表明,对新生儿在感染艾滋病病毒数小时或数天内使用抗逆转录病毒疗法,可能达到完全抑制艾滋病病毒的效果。然而在停药两年后,密西西比女孩今年7月再次被检测出艾滋病病毒,DNA分析发现,是来自女孩母亲身上的同一病毒株。
Carl W.Dieffenbach教授说:“在密西西比女孩这个案例中,最关键的问题是查清楚,HIV病毒藏在哪里,以及为什么又复发了”。抗逆转录病毒的药物能抑制血液中的病毒,但艾滋病毒在人体内有其躲避的藏身之处,如内脏和大脑。如果停止治疗,病毒就会从其藏身处出现,再次对人体发动攻击。Carl W.Dieffenbach教授表示,他个人认为现在需要找到更多类似病例,才能清楚地知道原因。
不过Carl W.Dieffenbach教授也带来了好消息,他告诉澎湃新闻,基因组剪辑技术已经进入到了动物实验及少量艾滋病病毒携带者实验当中。
今年7月,美国坦普尔大学研究人员发表声明,可以利用基因组编辑技术的精确剪切,将艾滋病毒从人类基因组中剔除。坦普尔大学的 Kamel Khalili等研究人员采用了CRISPR/CAS9 基因组剪辑系统,针对艾滋病病毒潜伏的多种细胞模型进行实验,比如小胶质细胞、T淋巴细胞等,实验结果证实,艾滋病病毒均被清除。
Carl W.Dieffenbach教授特别指出,这项技术未来的研究发展方向,将不仅仅是剪辑病毒这部分,更多地将是剪辑基因中的其他信息,使得被剪辑过的基因具有免疫病毒的能力。也就是说即使艾滋病病毒藏身在细胞中,也不会引起发病。Carl W.Dieffenbach教授告诉澎湃新闻:“现在遇到的挑战是,如何让被剪辑过的基因进入其他体内被感染的细胞当中”。



