自愈的奥秘
去年8月,被称为“旧金山患者”的洛伦·威伦伯格成为全世界第一例自然自愈的HIV感染者。这名患者的基因组中没有发现完整的HIV病毒序列,这表明她的免疫系统或已清除了HIV病毒库,科学家们将这种现象称为“清除性治愈”。于旭研究团队对这名患者的数十亿个细胞进行了测序,但未找到任何可用来制造新病毒的HIV序列。这是已知的第一例无须干细胞移植的清除性治愈病例,相关论文曾在线发表于2020年《自然》杂志上。
在这名新发现的“埃斯佩兰萨患者”体内超过11.9亿个血细胞和5亿个组织细胞中,科学家也没有检测到完整的HIV基因组。这意味着她可能已经消除了HIV病毒库,达到了“清除性治愈”状态。相关研究15日发表于《内科医学年鉴》。
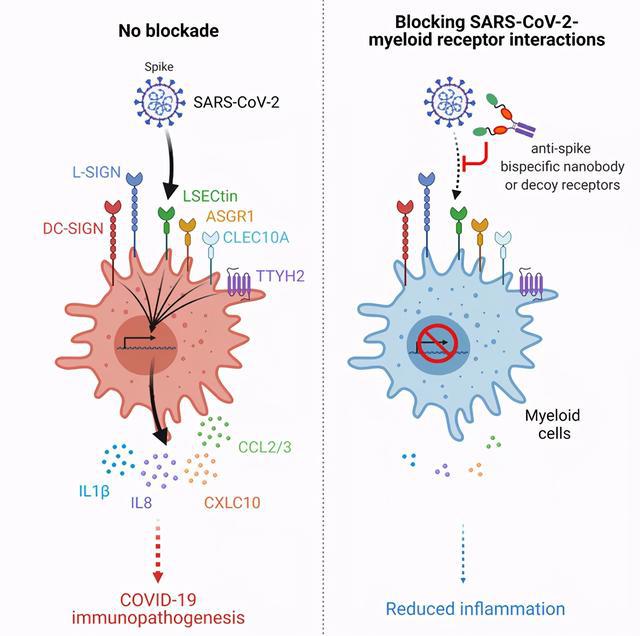
对于这种自愈现象的出现,美国著名HIV研究专家Steven Deeks教授,从感染初期的情况出发,向《每日经济新闻》记者解释道,“洛伦和埃斯佩兰萨患者可能都产生了一种免疫反应(包括杀手T细胞),能够对HIV的脆弱部分进行非常有效的靶向攻击,而且这些免疫细胞在感染初期的产生速度非常快。假如是这种情况的话,理论上HIV在能够扩散到全身之前就已经被控制住了。”Steven Deeks教授曾与于旭团队合作研究“旧金山患者”。
持续研究埃斯佩兰萨患者的Natalia Laufer也得出了相同结论,“有一种特定的杀手T细胞(即细胞毒性T细胞)反应,可能是在不服药的情况下也能抑制病毒繁殖的原因。”
两名自愈患者的出现,证明HIV自愈并不是孤例,还有更多的潜在自愈者,这为治愈艾滋病提供了新希望。“这些发现,特别是在识别出第二个案例后,表明存在一些可行的路径来帮助其他无法自愈的人实现清除性治愈,”于旭表示,这种实现的路径就是通过注射疫苗让接受ART治疗的患者最终能摆脱药物,实现自身免疫系统对病毒的抑制。
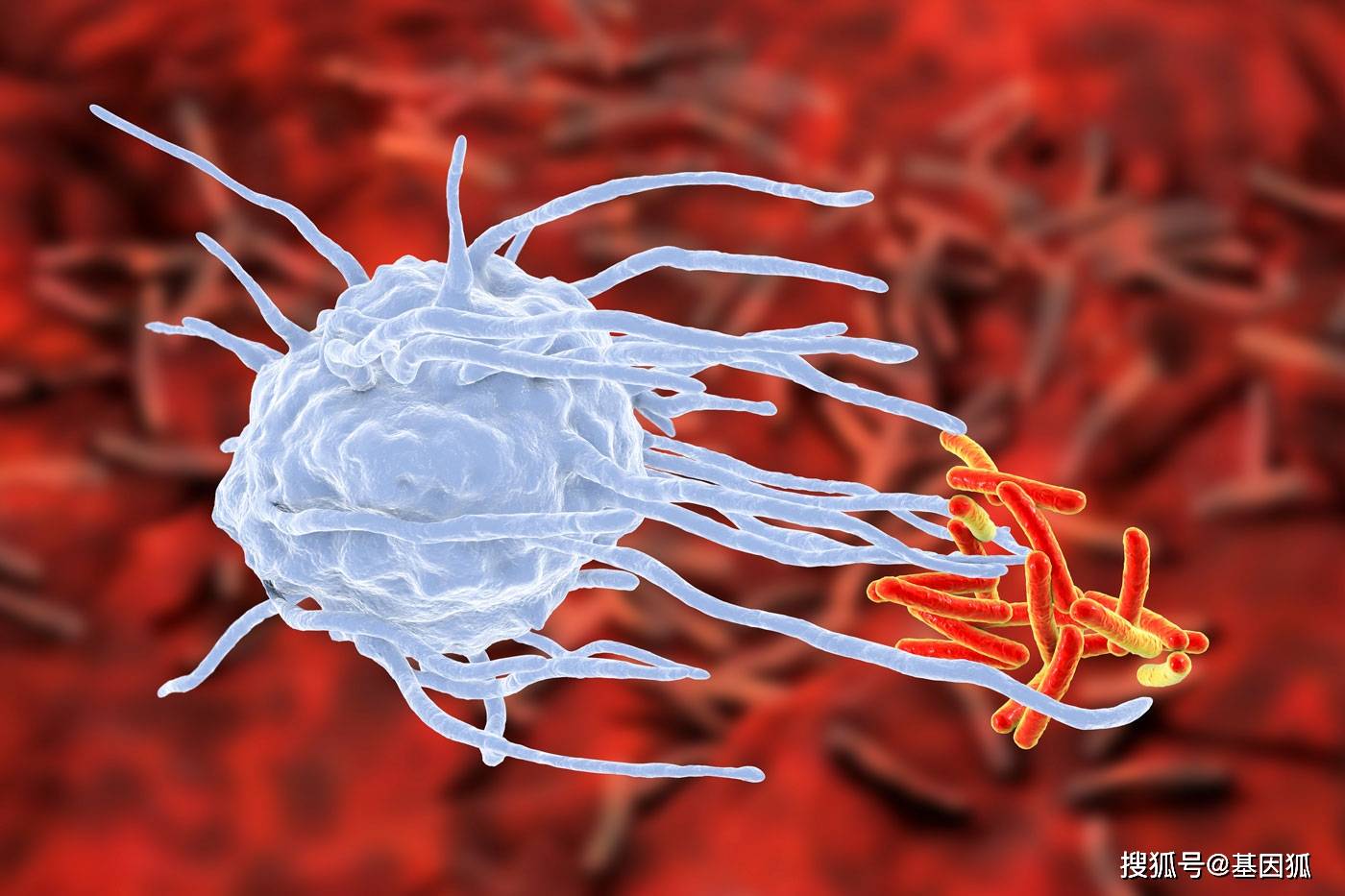
与此同时,研究人员也意识到了病例不足的事实。连晓东对《每日经济新闻》记者表示,下一步的研究重点是寻找更多的自愈病例,将他们和其他感染者做对比,希望能找出其背后的免疫机制原理。“下一步我们需要找到更多的自愈病例,两个患者的样本还是太小了,然后再通过和接受ART治疗的患者、‘精英控制者’进行对比,看看到底自愈患者有哪些不同之处。”
攻克艾滋病还有多远?
在全世界3800万HIV感染者中,目前只有两个人被公认为通过治疗手段实现了治愈,即2009年的“柏林患者”和2019年的“伦敦患者”。两人分别患有白血病和淋巴癌,在接受了捐赠者提供的具有抗HIV基因的干细胞移植之后,不仅治疗了癌症,而且在体内检测不出活跃的HIV。
两人的案例证明了通过治疗手段达到HIV治愈是可行的,但是移植过程昂贵且风险很高,捐赠者也很难找到。“伦敦患者”的主治医生、剑桥大学教授拉温德拉?古普塔表示,移植干细胞仅能作为最后的手段来治疗那些同时患有血液系统疾病的艾滋病患者,并不适用于所有病人。
在HIV感染人体的过程中,病毒将自己的基因组复制到细胞的DNA中,形成“病毒库”。病毒库可以躲避人体的免疫系统和药物的影响,源源不断地制造新的病毒出来。目前治疗HIV的主要方法是用抗逆转录病毒药物(ART)抑制病毒繁殖,将感染者长期控制在感染但不发病的状态。但这种治疗却不能消除病毒库的存在,一旦停药,HIV病毒很快就会反弹扩散。
而研究发现,在艾滋病患者中有一类特殊人群治愈艾滋病,被称为“精英控制者”,其免疫系统可在不使用ART的情况下控制病毒。也就是说,虽然他们体内仍然存在HIV病毒库,但一种称为“杀伤性T细胞”的免疫细胞可抑制病毒,因而无须进行药物治疗。

每200个HIV感染者中却有1个可以在不用药物的情况下抑制病毒增长。抑制了病毒生长但病毒库依然存在的患者则被称为“功能性治愈”。这类被称为“精英控制者”的人群是拉贡医学研究所于旭研究团队的长期研究对象。
连晓东告诉《每日经济新闻》记者,杀手T细胞的作用在“精英控制者”身上都能看到,但为何两名自愈患者却能达到清除病毒库的结果,还需要更多的研究。连晓东补充道,研究团队目前也在从广谱中和抗体的角度研究自愈患者的特殊性,但还没有结果出来。
“假如最终证实杀手T细胞就是自愈的原因,就可以设计和检验专门制造这类细胞的疫苗。目前已经有一些这类疫苗在开发中了治愈艾滋病,很多使用的就是新冠疫苗里的mRNA技术,”Steven Deeks教授补充道。
今年8月,成功研发了新冠疫苗的莫德纳公司宣布,将开展基于mRNA技术平台的HIV候选疫苗一期临床试验,并已经开始招募受试者。
记者|李孟林编辑|程鹏高涵 易启江 杜恒峰
校对|段炼



