今年CROI大会上,一例曾发布在顶尖期刊-《Nature》上的艾滋病病例引来各界关注,“柏林病人”不再孤独,世界第二位或将治愈的艾滋病患者-“伦敦病人”已经出现。尽管该病例许多巧合和意外无法复制,但也为探索功能性治愈铺平道路。
所谓功能性治愈即“在不使用抗病毒药物的情况下,完全控制HIV病毒复制和维持免疫功能”。
柏林病人
世界首位完全实现功能性治愈的艾滋病患者。1995年诊断出感染HIV, 2006年感染急性粒细胞性白血病(AML),接受两次造血干细胞骨髓移植手术,干细胞捐献者来自天然抵抗HIV的幸运儿(CCR5-△32基因变异)。第二次骨髓移植后不再服用抗病毒治疗药物,十几年过去了,体内也没有检测出艾滋病毒,在柏林过着平静的生活。
伦敦病人
第二例或将实现功能性治愈的艾滋病患者。2003年诊断为HIV阳性,2013年诊断患有霍奇金淋巴瘤,2016年接受干细胞移植手术,干细胞捐献者同样具有CCR5-△32纯合子突变,移植后510天停止cART(联合抗逆转录病毒治疗),停药后18个月病毒持续抑制。
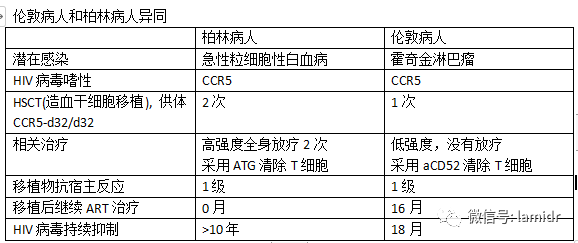
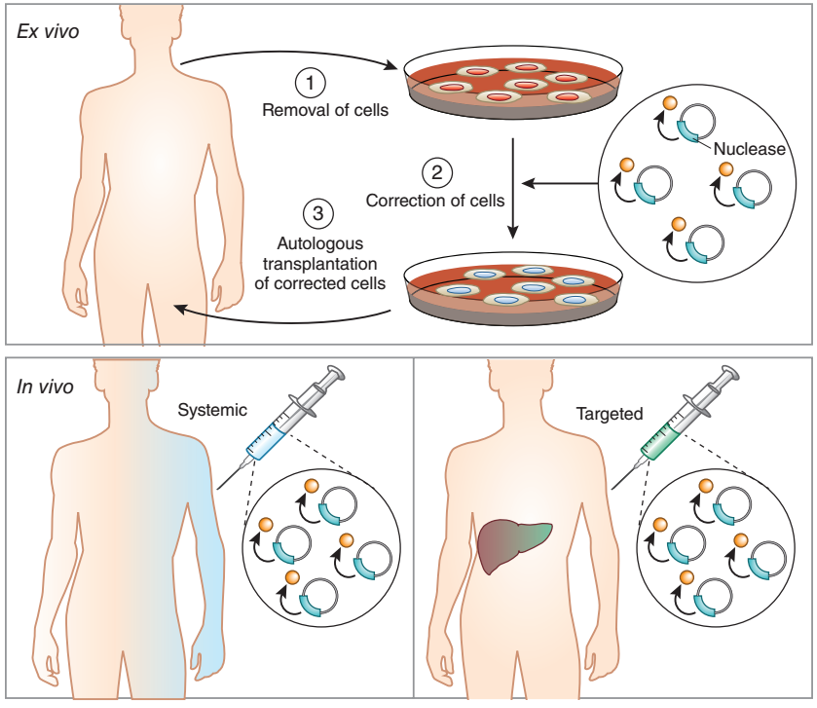
两名患者均接受CCR5-△32突变供体的干细胞,供体CD4+T细胞天然无法表达CCR5受体,进而阻断HIV病毒的感染。
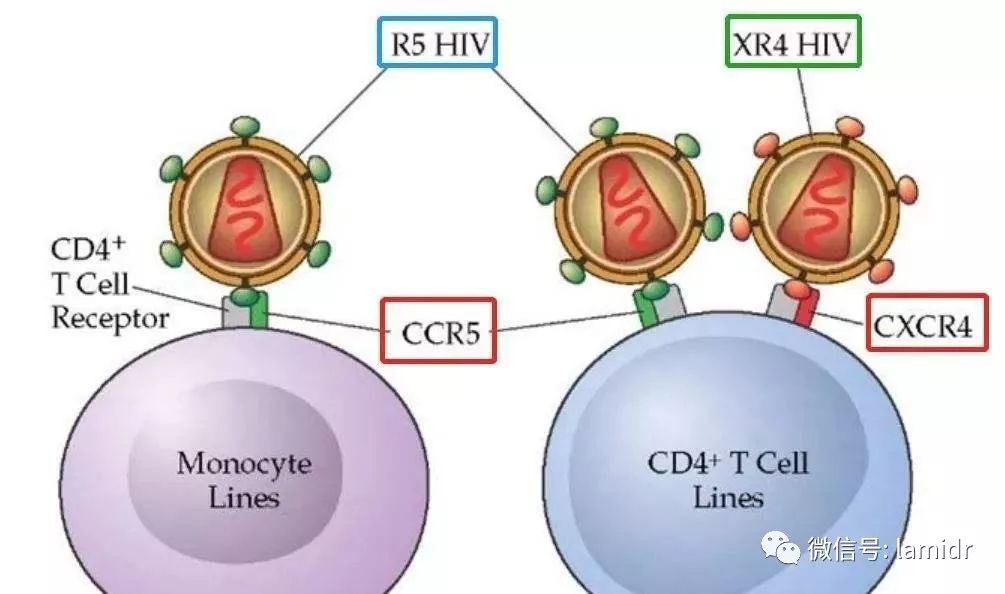
CCR5到底为何方神圣?为什么降低CCR5的表达,可以阻断病毒侵入CD4细胞?
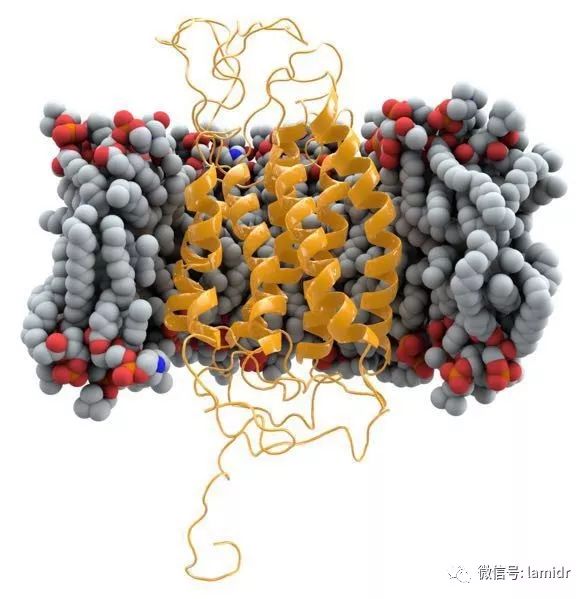
CCR5分子是一种7次跨膜蛋白艾滋病治愈,属于G蛋白偶联受体,具有趋化因子受体的功能,在人体的单核-巨噬细胞、树突状细胞、T细胞和NK细胞等多种免疫细胞表面均有表达,还在中枢神经系统(如海马等)及多种干细胞中表达。HIV病毒进入人体后,寻找靶细胞(CD4+T淋巴细胞),病毒表面的gp120与细胞CD4分子结合,但这种结合不够紧密,还需要“帮凶”-CCR5。
CCR5是一种趋化因子受体,可以在免疫细胞的细胞膜上打开口子,让病毒大举进入免疫细胞内。研究发现,1%欧洲白人拥有纯合的CCR5突变基因,基本不会感染艾滋病病毒;10%欧洲白人拥有杂合的CCR5突变基因,感染艾滋病病毒的概率也相对较低。柏林病人和伦敦病人接受的供体中均拥有CCR5突变基因,清除体内T细胞后,干细胞增殖,Western blot显示CD4细胞不表达CCR5,体外检测显示对R5型的HIV-1抵抗,对X4型的HIV依旧敏感。
如果伦敦病人能够实现功能性治愈,那么对CCR5基因的改造或治疗有希望成为艾滋病功能性治愈的突破口。
结语
柏林病人和伦敦病人的成功或许很难复制。全球几千万艾滋病患者,仅有少部分患者同时患有淋巴瘤或白血病,骨髓移植高风险高负担仅是患者最后救命的稻草,且找到合适供体本就不易,所以在任何情况下都无法推广使用。
虽然中国人的共受体以CXCR4或CXCR4/CCR5为主艾滋病治愈,HIV急性期还是主要通过CCR5途径进入免疫细胞,但该研究给我们带来了新的思路,能否通过体外编辑干细胞,从而提高体内CCR5突变的白细胞含量?可否通过基因编辑敲除CCR5基因?敲除CCR5基因后会不会造成其他功能损失?相关研究已经开展,有关研究的后续进展,详情请关注公众号后续推文,敬请期待。
参考文献:
1. Gupta RK et al. Sustained HIV-1 remission following homozygous CCR5 delta32 allogenic HSCT. CROI 4 – 7 March 2019, Seattle. Late breaker oral abstract 29 LB.
2.Gupta RK et al. HIV-1 remission following CCR5Δ32/Δ32 haematopoietic stem cell transplantation. Nature. DOI: 10.1038/s41586-019-1027-4.



