当地时间2月15日,美国加州大学洛杉矶分校的研究人员报告了全球第三例艾滋病治愈案例。
这名女性患者曾于2017年接受CCR5Δ32/Δ32突变的脐带血干细胞移植治疗。2020年10月,患者在停止使用抗逆转录病毒药物治疗后至今艾滋病治愈,都没有显示出任何艾滋病病毒(HIV)感染的迹象。无独有偶,此前被治愈的另外两例艾滋病病人——“柏林病人”和“伦敦病人”也都接受了CCR5Δ32/Δ32突变的骨髓造血干细胞移植治疗。
图源:视觉中国
锁住HIV入侵淋巴细胞的大门
“这三例患者都移植了CCR5Δ32/Δ32突变的造血干细胞,实现了艾滋病的临床治愈。但这并不意味着普通的造血干细胞就能终结艾滋病的流行。”解放军总医院第五医学中心感染病医学部主任医师孟繁平在接受科普时报记者专访时介绍,HIV专门攻击人体内CD4+T淋巴细胞,在淋巴细胞内增殖后再破坏该细胞,导致细胞裂解,从而继续感染并摧毁其他的淋巴细胞。
孟繁平说,HIV选择攻击CD4+T淋巴细胞,是因为在这种细胞的表面,有一种叫做趋化因子受体5(CCR5)的蛋白受体,它和该淋巴细胞表面的另一种蛋白受体CXCR4协同作用形成复合体,成为HIV进入淋巴细胞的两个共受体,充当着HIV进入淋巴细胞的大门的作用。当CCR5Δ32/Δ32这一基因发生突变时,会导致淋巴细胞表面CCR5蛋白不表达,这就相当于把HIV入侵淋巴细胞的大门锁上了。
“这三例病人很幸运,因为他们找到了CCR5Δ32/Δ32自然突变的供体,并且跟自己的配型也适合。世界上天生带有CCR5Δ32/Δ32突变(野生型突变)的人非常稀少,且大部分都在北欧国家。也有10%-18%的欧洲人仅仅只携带一个Δ32突变,但这并不能防止HIV感染,只会减少感染风险并延缓艾滋病进展。”孟繁平说。

威尔康奈尔医学院的研究人员 图:Benjamin Ryan
“功能性治愈”艾滋病新策略
既然野生型CCR5Δ32/Δ32突变的人群很小,能不能采用基因编辑的方法人为制造基因突变呢?
孟繁平说,我国在这个方面确实做出了很多有意义的尝试。
2017年,北京大学-清华大学生命科学联合中心邓宏魁研究组利用“基因剪刀”对造血干细胞进行CCR5基因编辑后,将其回输到一名患有白血病合并艾滋病的患者体内。经过长达19个月的随访发现,患者的白血病处于持续完全缓解状态,在短暂停止服用抗HIV病毒药物期间,CCR5基因编辑的T细胞表现出一定程度抵御HIV感染的能力。
2019年,邓宏魁研究组、首都医科大学附属北京佑安医院吴昊研究组以及解放军总医院第五医学中心陈虎课题组发表了题为《利用CRISPR基因编辑的成体造血干细胞在患有艾滋病合并急性淋巴细胞白血病患者中的长期重建》的研究论文。这意味着艾滋病治愈,通过基因编辑敲除成体造血干细胞上的CCR5基因,再将编辑后的细胞移植到艾滋病患者体内的方式,有可能成为“功能性治愈”艾滋病的新策略。
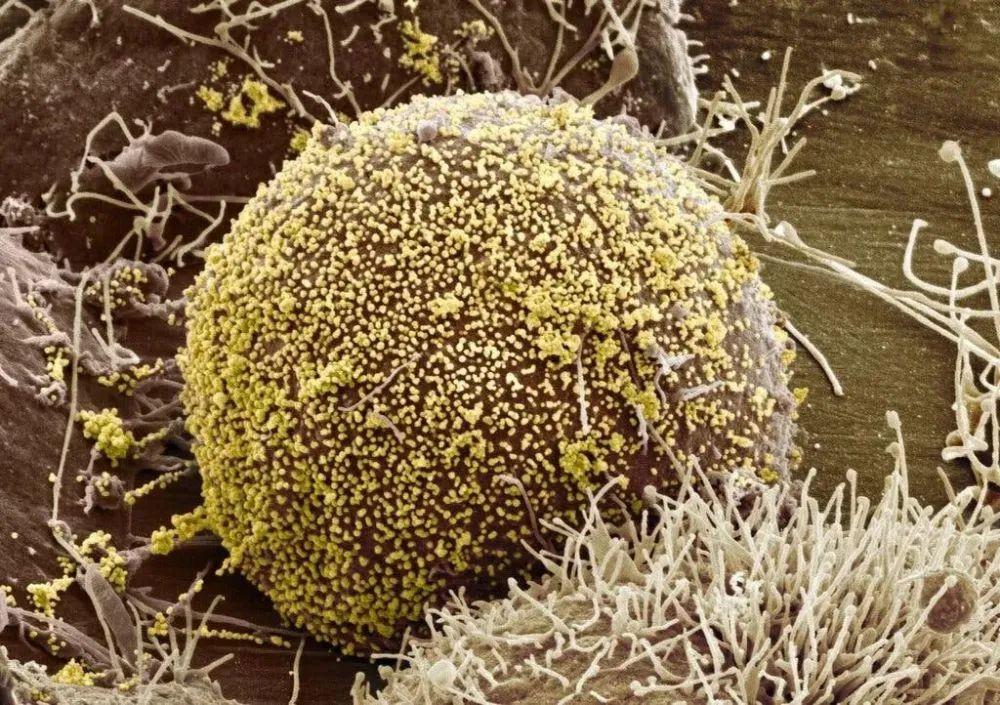
扫描电镜图下的HIV病毒颗粒(黄色)Thomas Deerinck, NCMIR/Science Source
还不能成为HIV常规治疗手段
“但是,通过基因编辑技术制造CCR5Δ32/Δ32突变仍然面临很多难题。比如,基因编辑还做不到对CCR5进行百分之百的纯化,HIV仍然可以通过残留的正常型CCR5进入人体的淋巴细胞,从而导致感染。而且,即使在体外能做到CCR5百分之百的纯化,造血干细胞在进入体内后也面临许多不确定的因素,可能导致细胞发生改变。” 孟繁平说,“除此之外,造血干细胞移植前还需要先把患者原有的免疫系统彻底摧毁,如果摧毁不彻底,还有可能导致肿瘤或血液病的二次复发。”
孟繁平提醒,即使造血干细胞移植成功,供体的T淋巴细胞也会攻击受者的各个组织器官,从而导致移植物抗宿主病的发生,出现一系列症状。“总的来说,造血干细胞移植属于一种成本大、风险高的治疗方式,在治疗HIV上,造血干细胞移植的风险远大于获益,不能成为常规治疗手段。但对那些患有艾滋病同时又合并恶性肿瘤或血液疾病的患者而言,选择CCR5Δ32/Δ32突变的造血干细胞移植也不失为一种权衡利弊后的有益尝试。”



